Das System der Patentlaufzeitverlängerung geht auf den US-amerikanischen Drug Price Competition and Patent Term Restoration Act von 1984 (Hatch-Waxman Act) zurück. In der Folgezeit etablierten auch viele Länder oder Regionen wie Japan, Südkorea, die Europäische Union und Kanada ähnliche Systeme, um den Verlust der Patentschutzfrist zu kompensieren, der durch die langwierigen Zulassungsverfahren für innovative Medikamente entstand.
Am 15. Januar 2020 unterzeichnete China ein Wirtschafts- und Handelsabkommen mit den Vereinigten Staaten, in dem vereinbart wurde, dem chinesischen Patentgesetz ein System zur Verlängerung der Patentlaufzeit hinzuzufügen, um Verluste auszugleichen, die durch unangemessene Verzögerungen bei der Patentgenehmigung oder der Zulassung von Arzneimitteln entstehen. Im Juni 2021 trat das überarbeitete Patentgesetz offiziell in Kraft und mit der offiziellen Umsetzung des Systems zur Verlängerung der Patentlaufzeit begann China. Die neuen Durchführungsbestimmungen und Patentprüfungsrichtlinien traten am 20. Januar 2024 in Kraft und enthalten Einzelheiten zu den Durchführungsbestimmungen zur Patentlaufzeitverlängerung in China.
PTE Übersicht
- Artikel 42 Absatz 3 des überarbeiteten Patentgesetzes sieht vor, dass die China National Intellectual Property Administration (CNIPA) zum Ausgleich des Zeitaufwands für die Zulassung neuer Medikamente auf Antrag des Patentinhabers die Laufzeit von Erfindungspatenten für neue Medikamente, deren Vermarktung in China bereits zugelassen ist, verlängern kann. Die Verlängerung der Patentlaufzeit darf fünf Jahre nicht überschreiten, und die gesamte effektive Patentlaufzeit nach der Verlängerung darf 14 Jahre ab dem Datum der Marktzulassung des neuen Arzneimittels nicht überschreiten.
- Mit dieser Regelung soll ein Ausgleich zwischen den hohen Kosten und langen Entwicklungszyklen innovativer Medikamente geschaffen werden. So soll sichergestellt werden, dass die Pharmaunternehmen ihre Investitionen in Forschung und Entwicklung während der Patentschutzdauer angemessen zurückgewinnen können. Gleichzeitig sollen mehr Arzneimittelinnovationen gefördert und die Begeisterung der Unternehmen für Forschung und Entwicklung gesteigert werden.
Für die Patentlaufzeitverlängerung (PTE) geeignete Arzneimittel
- Die Verlängerung der Patentlaufzeit gilt für Produktpatente, Patente auf Herstellungsverfahren und Patente auf die medizinische Verwendung im Zusammenhang mit den in den „neuen Arzneimitteln“ enthaltenen aktiven pharmazeutischen Inhaltsstoffen (APIs). „Neue Arzneimittel“ bezieht sich auf innovative Arzneimittel und bestimmte verbesserte neue Arzneimittel gemäß der Definition in den Arzneimittelgesetzen und -vorschriften der National Medical Products Administration (NMPA). Damit ein Arzneimittel in China als „neues Arzneimittel“ für eine Patentlaufzeitverlängerung in Frage kommt, muss das Arzneimittel weltweit neu sein. Dies bedeutet, dass in China ein Antrag auf Marktzulassung eines neuen Arzneimittels (NDA) eingereicht werden muss, bevor in anderen Ländern eine Marktzulassung erteilt wird. Es ist jedoch nicht erforderlich, dass der NDA in China genehmigt wird, bevor er in anderen Ländern genehmigt werden kann.
Innovative Arzneimittel, die die PTE-Bedingungen erfüllen:
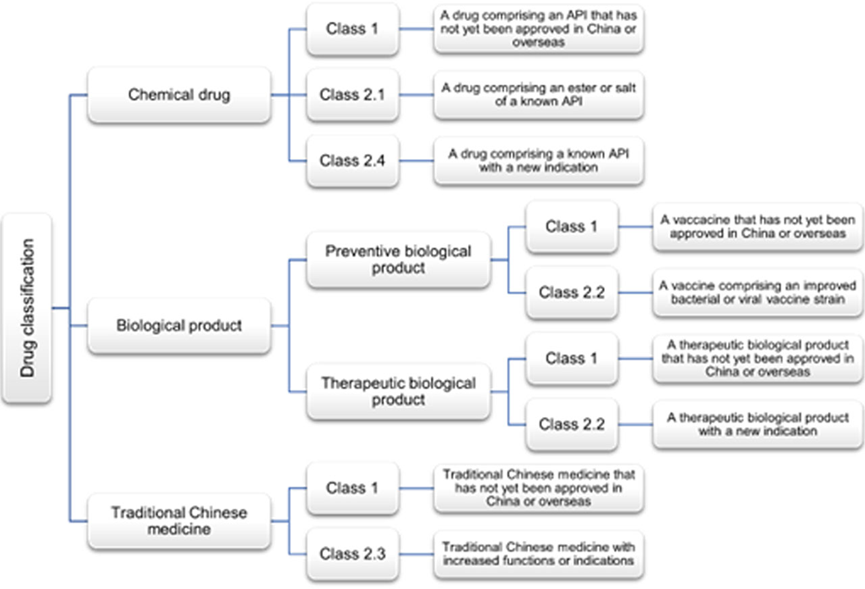
- Gemäß den aktuellen Arzneimittelklassifizierungsvorschriften der NMPA gelten innovative Arzneimittel als Arzneimittel der Klasse 1 und müssen weltweit neu sein. Zu den infrage kommenden innovativen Arzneimitteln zählen die folgenden Medikamente, die in China oder im Ausland noch nicht zugelassen sind:
- Chemische Medikamente;
- vorbeugende biologische Produkte – Impfstoffe;
- Therapeutische biologische Produkte;
- traditionelle chinesische Medizin.
Verbesserte neue Medikamente, die die PTE-Bedingungen erfüllen:
- Verbesserte neue Arzneimittel müssen auch weltweit neu sein und sind gemäß den Arzneimittelklassifizierungsvorschriften der NMPA auf die folgenden Arzneimittel beschränkt:
- Ester oder Salze bekannter pharmazeutischer Wirkstoffe der Klasse 2.1 für chemische Arzneimittel;
- Bekannte APIs mit neuen Indikationen in chemischen Arzneimitteln der Klasse 2.4;
- Impfstoffe mit veränderten Bakterien- oder Virenstämmen der Kategorie 2.2 der vorbeugenden biologischen Produkte;
- Biologische Therapeutika mit neuen Indikationen der Kategorie 2.2 der biologischen Therapeutika;
- Traditionelle chinesische Arzneimittel der Kategorie 2.3 mit erweiterten Funktionen oder Indikationen.
Arzneimittel, die nicht für den PTE in Frage kommen:
- Gemäß der oben genannten Definition eines „neuen Arzneimittels“ erfüllen importierte Arzneimittel (d. h. Arzneimittel, die bei der Beantragung einer Marktzulassung in China bereits im Ausland vermarktet wurden) die PTE-Bedingungen nicht. Hierzu zählen insbesondere chemische Arzneimittel der Klasse 5.1, vorbeugende biologische Produkte der Klassen 3.1 und 3.2 sowie therapeutische biologische Produkte der Klassen 3.1 und 3.2.
Diese Bestimmungen stellen sicher, dass nur Arzneimittel, die weltweit die ersten ihrer Art sind oder deutlich verbessert wurden, für eine Verlängerung der Patentlaufzeit in Frage kommen. Auf diese Weise werden echte Innovationen und qualitativ hochwertige Verbesserungen gefördert.
Die für eine Patentlaufzeitverlängerung (PTE) in Frage kommenden Arzneimittelkategorien sind in der folgenden Tabelle zusammengefasst:
Frist für die PTE-Bewerbung
- Der Patentinhaber oder sein Vertreter muss innerhalb von drei Monaten nach Erhalt der Marktzulassung für ein Arzneimittel einen Antrag auf Verlängerung der Patentlaufzeit (PTE) einreichen und die offizielle Gebühr bezahlen. Der Antrag muss nach der Genehmigung durch den Zulassungsinhaber gestellt werden.
Voraussetzungen für den Erwerb des PTE
- Um einen PTE in China zu erhalten, müssen folgende Voraussetzungen erfüllt sein:
- Der Erteilungstag des Patents sollte vor dem Zulassungsdatum des Arzneimittels liegen;
- Beim Einreichen eines PTE-Antrags sollte das Patent gültig sein;
- Für das Patent wurde noch kein PTE erteilt.
- Die Patentansprüche sollten technische Lösungen in Bezug auf das Arzneimittel enthalten; diese technischen Lösungen umfassen die Struktur, Zusammensetzung und Dosierung des zugelassenen neuen Arzneimittels sowie das zugelassene Herstellungsverfahren und die Indikationen;
- Wenn das Arzneimittel durch mehrere Patente geschützt ist, kann nur die Laufzeit eines Patents verlängert werden;
- Wenn ein Patent mehrere Arzneimittel abdeckt, kann ein PTE nur für eines der Arzneimittel beantragt werden.
Berechnung des PTE-Zeitlimits
- Beim PTE handelt es sich um eine zusätzliche Berechnung zusätzlich zu einer etwaigen Patentlaufzeitanpassung (PTA). Die Berechnung des PTE sollte nach der PTA-Entscheidung durchgeführt werden. Aufgrund der unterschiedlichen Entschädigungsgründe kann es zu einer Kumulation der Entschädigungszeiträume von PTA und PTE kommen.
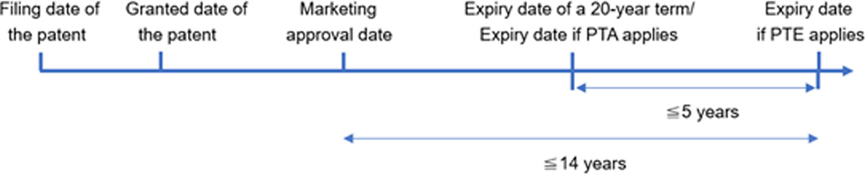
- Der PTE wird berechnet, indem von der Anzahl der Tage zwischen dem chinesischen Patentanmeldedatum und dem chinesischen Arzneimittelzulassungsdatum fünf Jahre abgezogen werden. Gleichzeitig muss das PTE die folgenden beiden Anforderungen erfüllen: Die maximale PTE-Laufzeit beträgt fünf Jahre und die gesamte effektive Patentlaufzeit nach der Marktzulassung des Arzneimittels darf 14 Jahre nicht überschreiten.
Prüfung des PTE-Antrags
- Bevor der Prüfer über die Gewährung einer PTE-Entschädigung entscheidet, gibt er dem Patentinhaber mindestens einmal die Gelegenheit, Anmerkungen oder Änderungen vorzunehmen. Wenn die Voraussetzungen für das PTE erfüllt sind, erteilt das CNIPA das PTE, gibt die Anzahl der Tage bekannt, um die die Patentlaufzeit verlängert wird, und veröffentlicht Informationen wie den Arzneimittelnamen, zugelassene Indikationen und das ursprüngliche und neue Ablaufdatum des Patents im Patentblatt. Ist der Patentinhaber oder ein interessierter Dritter mit der Entscheidung des CNIPA nicht zufrieden, kann er eine Verwaltungsüberprüfung einleiten.
Schutzumfang während der PTE-Periode
- Da der Zweck des PTE darin besteht, den Zeitaufwand für die Marktzulassung neuer Arzneimittel zu kompensieren, ist es notwendig, das zugelassene neue Arzneimittel direkt mit der technischen Lösung des Arzneimittelpatents zu verknüpfen, für das der PTE beantragt wird. Die technischen Lösungen im Zusammenhang mit neuen Medikamenten dienen als Brücke zwischen den auf den Markt gebrachten neuen Medikamenten und den Medikamentenpatenten, für die PTE beantragt wird.
- Der Schutzumfang eines PTE ist enger als der eines Patents selbst und beschränkt sich auf neue Arzneimittel mit zugelassenen Indikationen. Dies bedeutet, dass der Schutzumfang eines PTE Folgendes umfasst:
- Neue Arzneimittel in Produktansprüchen für zugelassene Indikationen;
- Neue Arzneimittel mit zugelassenen Indikationen im Rahmen medizinischer Verwendungsansprüche;
- Der Herstellungsprozess neuer Arzneimittel für zugelassene Indikationen wird von der NMPA aufgezeichnet.
- Eine neue Indikation kann einen neuen PTE rechtfertigen, der Umfang des erhaltenen PTE erstreckt sich jedoch nur auf die neue Indikation, auf der der PTE basiert, und nicht auf früher oder später zugelassene Indikationen.
- Daher sollte der Patentinhaber bei der Einreichung eines PTE-Antrags Materialien zur Bestimmung des Schutzumfangs des PTE bereitstellen, z. B. Materialien, die die Zusammensetzung des zugelassenen Arzneimittels zeigen, Materialien, die die Indikationen des zugelassenen Arzneimittels zeigen, und Materialien zum von der NMPA zugelassenen Arzneimittelherstellungsprozess.
abschließend
Innovative Pharmaunternehmen sollten das chinesische PTE-System aktiv nutzen, um eine Verlängerung der Patentlaufzeit zu beantragen. Beim Einreichen eines PTE-Antrags sollten innovative Pharmaunternehmen alle Faktoren berücksichtigen, etwa die Art und den Umfang der Ansprüche, die Stabilität des Patents, die Durchsetzung des Patents, den Umfang des PTE und die Regel „ein Medikament, ein Patent, ein PTE“, um die Verlängerung der Patentlaufzeit für ein oder mehrere Patente zu maximieren und zu rationalisieren.
Für Generikahersteller führt eine Verlängerung der Patentlaufzeit für innovative Medikamente zwangsläufig zu einer Verzögerung der Markteinführung von Generika, was erhebliche Auswirkungen auf viele Generikahersteller in China hat. Generikahersteller sollten die Patentablaufdaten innovativer Pharmaunternehmen genau im Auge behalten und eine strategische Planung zur Rationalisierung des NDA-Prozesses planen. Gegebenenfalls können Generikahersteller auch die Einreichung von Anträgen auf Nichtigerklärung der Patente innovativer Pharmaunternehmen in Erwägung ziehen.
Eine verzögerte Markteinführung von Generika führt zu einer Erhöhung der Arzneimittelgebühren. Wenn es darum geht, die Gewinne innovativer Pharmaunternehmen und Generikahersteller auszugleichen, kommt den Patentanmeldern eine besondere Bedeutung zu. Dieses Gleichgewicht wurde bei der Formulierung des Patentgesetzes und der Ausführungsbestimmungen zum PTE berücksichtigt und spiegelt sich in mehreren Anforderungen zum Erhalt eines PTE wider. Zu den Anforderungen gehört beispielsweise, dass nur Patente, die noch kein PTE erhalten haben, für ein PTE infrage kommen. Wenn ein Arzneimittel durch mehrere Patente geschützt ist, kann nur ein Patent verlängert werden. Und wenn ein Patent mehrere Arzneimittel abdeckt, kann nur für eines der Arzneimittel ein PTE beantragt werden. Darüber hinaus ist festgelegt, dass die maximale Laufzeit des PTE fünf Jahre beträgt und die gesamte effektive Patentlaufzeit nach der Marktzulassung des Arzneimittels 14 Jahre nicht überschreiten darf. Mit diesen Anforderungen wird nicht nur wirksam eine doppelte Vergütung der Patentlaufzeiten innovativer Pharmaunternehmen vermieden, sondern auch eine übermäßige Verlängerung der Patentlaufzeiten verhindert.
 | Get exact prices For the country / regionE-mail: mail@yezhimaip.com |

