نشأ نظام تمديد مدة براءة الاختراع من قانون المنافسة على أسعار الأدوية واستعادة مدة براءة الاختراع الأمريكي لعام 1984 (قانون هاتش-واكسمان). وفي وقت لاحق، أنشأت العديد من البلدان أو المناطق مثل اليابان وكوريا الجنوبية والاتحاد الأوروبي وكندا أنظمة مماثلة للتعويض عن فقدان فترة حماية براءات الاختراع الناجمة عن عملية الموافقة الطويلة على الأدوية المبتكرة.
في 15 يناير 2020، وقعت الصين اتفاقية اقتصادية وتجارية مع الولايات المتحدة، وافقت بموجبها على إضافة نظام تمديد مدة براءة الاختراع إلى قانون براءات الاختراع الصيني للتعويض عن الخسائر الناجمة عن التأخيرات غير المعقولة في عملية ترخيص براءات الاختراع أو الموافقة على تسويق الأدوية. في يونيو 2021، دخل قانون براءات الاختراع المعدل حيز التنفيذ رسميًا، وبدأ تنفيذ نظام تمديد مدة براءة الاختراع رسميًا في الصين. دخلت قواعد التنفيذ الجديدة وإرشادات فحص براءات الاختراع حيز التنفيذ في 20 يناير 2024، وهي توضح قواعد التنفيذ لتمديد مدة براءة الاختراع في الصين.
نظرة عامة على اختبار PTE
- تنص الفقرة 3 من المادة 42 من قانون براءات الاختراع المعدل على أنه من أجل تعويض الوقت المستغرق في الموافقة على تسويق دواء جديد، يجوز للإدارة الوطنية للملكية الفكرية في الصين (CNIPA)، بناءً على طلب مالك براءة الاختراع، تمديد مدة براءات الاختراع المتعلقة بالأدوية الجديدة التي تمت الموافقة على تسويقها في الصين. ولا يجوز أن يتجاوز تمديد مدة براءة الاختراع خمس سنوات، ولا يجوز أن يتجاوز إجمالي مدة براءة الاختراع الفعلية بعد التمديد 14 سنة من تاريخ الموافقة على تسويق الدواء الجديد.
- تهدف هذه اللائحة إلى تحقيق التوازن بين التكلفة العالية والدورة الطويلة لتطوير الأدوية المبتكرة، وضمان قدرة شركات الأدوية على استرداد استثماراتها في البحث والتطوير بشكل معقول خلال فترة حماية براءة الاختراع، مع تشجيع المزيد من الابتكارات الدوائية الجديدة وزيادة حماس الشركات للبحث والتطوير.
الأدوية التي يمكن تمديد مدة براءة الاختراع الخاصة بها (PTE)
- ينطبق تمديد مدة براءة الاختراع على براءات اختراع المنتج وبراءات اختراع عملية التحضير وبراءات اختراع الاستخدام الطبي المتعلقة بالمكونات الصيدلانية الفعالة (APIs) الموجودة في "الأدوية الجديدة". تشير عبارة "الأدوية الجديدة" إلى الأدوية المبتكرة وبعض الأدوية الجديدة المحسنة كما هو محدد في قوانين ولوائح تنظيم الأدوية الصادرة عن الإدارة الوطنية للمنتجات الطبية (NMPA). لكي يكون منتج دوائي مؤهلاً باعتباره "دواءً جديدًا" لتمديد مدة براءة الاختراع في الصين، يجب أن يكون المنتج الدوائي جديدًا على المستوى العالمي، وهذا يعني أنه يجب تقديم طلب دواء جديد (NDA) في الصين قبل الحصول على موافقة التسويق في بلدان أخرى. ومع ذلك، ليس من الضروري أن تتم الموافقة على NDA في الصين قبل أن تتم الموافقة عليها في بلدان أخرى.
الأدوية المبتكرة التي تلبي شروط PTE:
- وفقًا لأنظمة تصنيف الأدوية الحالية التابعة لـ NMPA، تشير الأدوية المبتكرة إلى أدوية الفئة 1 ويجب أن تكون جديدة على مستوى العالم. وتشمل الأدوية المبتكرة المؤهلة الأدوية التالية التي لم تتم الموافقة عليها بعد في الصين أو في الخارج:
- المخدرات الكيميائية؛
- المنتجات البيولوجية الوقائية – اللقاحات؛
- المنتجات البيولوجية العلاجية؛
- الطب الصيني التقليدي.
تحسين الأدوية الجديدة التي تلبي شروط PTE:
- ويجب أن تكون الأدوية الجديدة المحسنة جديدة أيضًا على المستوى العالمي، ووفقًا لقواعد تصنيف الأدوية التابعة للهيئة الوطنية للأدوية، تقتصر على الأدوية التالية:
- إسترات أو أملاح المكونات الفعالة المعروفة في الفئة 2.1 من الأدوية الكيميائية؛
- المكونات الفعالة المعروفة ذات المؤشرات الجديدة في الأدوية الكيميائية من الفئة 2.4؛
- اللقاحات التي تحتوي على سلالات بكتيرية أو فيروسية معدلة من الفئة 2.2 من المنتجات البيولوجية الوقائية؛
- المنتجات البيولوجية العلاجية ذات المؤشرات الجديدة في الفئة 2.2 من المنتجات البيولوجية العلاجية؛
- الأدوية الصينية التقليدية في الفئة 2.3 التي لها وظائف أو مؤشرات متزايدة.
الأدوية التي لا تنطبق عليها معايير اختبار PTE:
- وفقًا للتعريف أعلاه لـ "الدواء الجديد"، فإن الأدوية المستوردة (أي الأدوية التي تم تسويقها في الخارج عند التقدم بطلب للحصول على موافقة التسويق في الصين) لا تلبي شروط PTE. وتشمل هذه الفئات على وجه التحديد الأدوية الكيميائية من الفئة 5.1، والمنتجات البيولوجية الوقائية من الفئة 3.1 و3.2، والمنتجات البيولوجية العلاجية من الفئة 3.1 و3.2.
وتضمن هذه الأحكام أن الأدوية التي تعد الأولى من نوعها على مستوى العالم أو التي تم تحسينها بشكل كبير هي فقط المؤهلة لتمديد مدة براءة الاختراع، وبالتالي تشجيع الابتكار الحقيقي والتحسينات عالية الجودة.
يتم تلخيص فئات الأدوية المؤهلة لتمديد مدة براءة الاختراع (PTE) في الجدول أدناه:
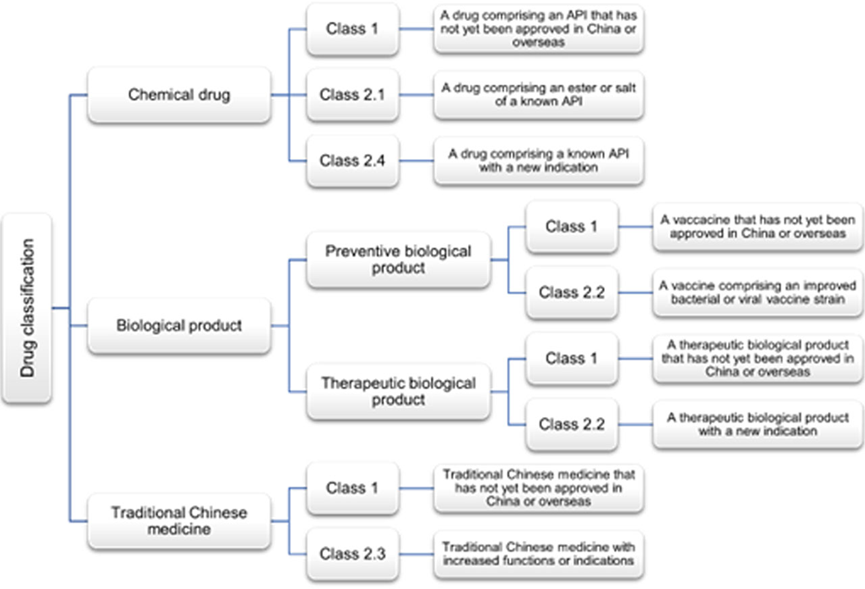
الحد الزمني للتقديم لاختبار PTE
- يجب على مالك براءة الاختراع أو وكيله تقديم طلب تمديد مدة براءة الاختراع (PTE) خلال ثلاثة أشهر من الحصول على موافقة التسويق للدواء ودفع الرسوم الرسمية. يجب تقديم الطلب بعد الحصول على موافقة حامل تصريح التسويق.
متطلبات الحصول على اختبار PTE
- للحصول على اختبار PTE في الصين، يجب استيفاء المتطلبات التالية:
- يجب أن يكون تاريخ منح براءة الاختراع أسبق من تاريخ الموافقة على الدواء؛
- عند تقديم طلب PTE، يجب أن تكون براءة الاختراع في حالة صالحة؛
- لم تحصل براءة الاختراع على PTE بعد؛
- يجب أن تتضمن مطالبات براءة الاختراع حلولاً تقنية تتعلق بالدواء؛ وتشمل هذه الحلول التقنية هيكل وتركيبة وجرعة الدواء الجديد المعتمد، بالإضافة إلى عملية التصنيع المعتمدة والمؤشرات؛
- إذا كان الدواء محميًا ببراءات اختراع متعددة، فلا يمكن تمديد مدة براءة اختراع واحدة إلا؛
- إذا كانت براءة الاختراع تغطي أدوية متعددة، فلا يمكن التقدم بطلب الحصول على براءة اختراع إلا لدواء واحد من هذه الأدوية.
حساب الحد الزمني لاختبار PTE
- يعد PTE حسابًا إضافيًا بالإضافة إلى أي تعديل في مدة براءة الاختراع (PTA) ويجب إجراء حساب PTE بعد اتخاذ قرار PTA. بسبب أسباب التعويض المختلفة، يمكن تجميع فترات التعويض الخاصة بـ PTA و PTE.
- يتم حساب PTE عن طريق طرح خمس سنوات من عدد الأيام بين تاريخ طلب براءة الاختراع الصيني وتاريخ موافقة تسويق الدواء في الصين. وفي الوقت نفسه، يجب أن يفي PTE بالمتطلبين التاليين: الحد الأقصى لمدة PTE هو خمس سنوات، ويجب ألا يتجاوز إجمالي مدة براءة الاختراع الفعلية بعد الموافقة على الدواء للتسويق 14 عامًا.
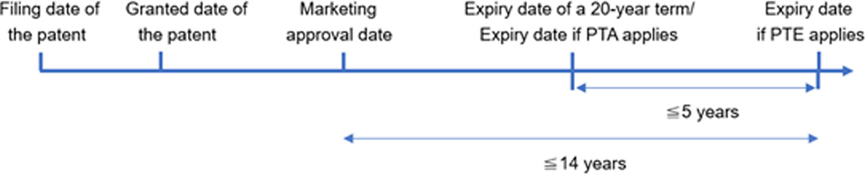
فحص طلب PTE
- قبل اتخاذ القرار بشأن منح تعويض PTE، سيمنح الفاحص مالك براءة الاختراع فرصة واحدة على الأقل لتقديم التعليقات أو التعديلات. إذا تم استيفاء متطلبات PTE، فسوف تمنح CNIPA PTE، وتخطر بعدد الأيام التي يتم فيها تمديد مدة براءة الاختراع، وتنشر معلومات مثل اسم الدواء، والمؤشرات المعتمدة، وتواريخ انتهاء الصلاحية الأصلية والجديدة لبراءة الاختراع في الجريدة الرسمية لبراءات الاختراع. في حالة عدم الرضا عن قرار الهيئة الوطنية للملكية الصناعية، يجوز لمالك براءة الاختراع أو لطرف ثالث مهتم رفع دعوى مراجعة إدارية.
نطاق الحماية خلال فترة PTE
- نظرًا لأن الغرض من PTE هو تعويض الوقت المستغرق في الموافقة على تسويق الأدوية الجديدة، فمن الضروري ربط الدواء الجديد المعتمد بشكل مباشر بالحل التقني لبراءة اختراع الدواء الذي يتم تطبيق PTE عليه. ستعمل الحلول التقنية المتعلقة بالأدوية الجديدة كجسر بين الأدوية الجديدة التي تم إطلاقها وبراءات اختراع الأدوية التي يتم تطبيق PTE عليها.
- إن نطاق حماية PTE أضيق من نطاق براءة الاختراع نفسها، ويقتصر على الأدوية الجديدة ذات المؤشرات المعتمدة، مما يعني أن نطاق حماية PTE يشمل:
- منتجات دوائية جديدة في مطالبات المنتجات للمؤشرات المعتمدة؛
- الأدوية الجديدة التي تمت الموافقة على مؤشرات استخدامها طبياً؛
- عملية تصنيع الأدوية الجديدة للمؤشرات المعتمدة المسجلة من قبل NMPA.
- قد يدعم مؤشر جديد اختبار PTE جديدًا، ولكن نطاق اختبار PTE الذي تم الحصول عليه سيغطي فقط المؤشر الجديد الذي يعتمد عليه اختبار PTE وليس أي مؤشرات تمت الموافقة عليها سابقًا أو لاحقًا.
- لذلك، عند تقديم طلب PTE، يجب على مالك براءة الاختراع تقديم المواد اللازمة لتحديد نطاق حماية PTE، مثل المواد التي توضح تركيبة الدواء المعتمد، والمواد التي توضح مؤشرات الدواء المعتمدة، والمواد المتعلقة بعملية تصنيع الدواء المعتمدة من قبل NMPA.
ختاماً
ينبغي لشركات الأدوية المبتكرة أن تستخدم بشكل نشط نظام PTE الصيني لتقديم طلبات تمديد مدة براءة الاختراع. عند تقديم طلب PTE، يجب على شركات الأدوية المبتكرة النظر في جميع العوامل، مثل نوع المطالبات، ونطاق المطالبات، واستقرار براءة الاختراع، وتنفيذ براءة الاختراع، ونطاق PTE وقاعدة "دواء واحد، براءة اختراع واحدة، PTE واحد" لتعظيم وترشيد تمديد مدة براءة الاختراع لبراءة اختراع واحدة أو أكثر.
بالنسبة لشركات الأدوية العامة، فإن تمديد مدة براءة اختراع الأدوية المبتكرة سوف يؤدي حتما إلى تأخير الوقت اللازم لدخول الأدوية العامة إلى السوق، وبالتالي سيكون له تأثير كبير على العديد من شركات الأدوية العامة في الصين. ينبغي لشركات الأدوية العامة أن تولي اهتماما وثيقا لتاريخ انتهاء صلاحية براءات الاختراع لشركات الأدوية المبتكرة والتخطيط الاستراتيجي لتبسيط عملية طلب تسجيل منتج جديد. وإذا لزم الأمر، قد تنظر شركات الأدوية العامة أيضًا في تقديم طلبات لإبطال براءات اختراع شركات الأدوية المبتكرة.
إن التأخر في إدخال الأدوية الجنيسة إلى السوق من شأنه أن يؤدي إلى زيادة الرسوم المفروضة على مستخدمي الأدوية. ويعتبر المتقدمون للحصول على براءات الاختراع مهمين بشكل خاص عند السعي إلى تحقيق التوازن بين أرباح شركات الأدوية المبتكرة وشركات الأدوية العامة. وقد تم أخذ هذا التوازن في الاعتبار عند صياغة قانون براءات الاختراع واللائحة التنفيذية فيما يتعلق بـ PTE وينعكس في العديد من المتطلبات للحصول على PTE. على سبيل المثال، تتضمن المتطلبات أن براءات الاختراع التي لم تحصل على PTE فقط هي المؤهلة للحصول على PTE؛ وإذا كان الدواء محميًا ببراءات اختراع متعددة، فلا يمكن تمديد سوى براءة اختراع واحدة؛ وإذا كانت براءة الاختراع تغطي أدوية متعددة، فلا يمكن للبراءة التقدم بطلب للحصول على PTE إلا لأحد الأدوية. كما ينص أيضًا على أن الحد الأقصى لمدة براءة الاختراع هو خمس سنوات، ولا يجوز أن يتجاوز إجمالي مدة براءة الاختراع الفعلية بعد موافقة الدواء على التسويق 14 عامًا. ولا تساعد هذه المتطلبات بشكل فعال على تجنب التعويض المزدوج لشروط براءات الاختراع لشركات الأدوية المبتكرة فحسب، بل تمنع أيضًا التمديد المفرط لشروط براءات الاختراع.
联系咨询
 | Get exact prices For the country / regionE-mail: mail@yezhimaip.com |

