특허 기간 연장 제도는 1984년 미국 의약품 가격 경쟁 및 특허 기간 회복법(해치-왁스만법)에서 유래되었습니다. 이후 일본, 한국, 유럽연합, 캐나다 등 많은 국가나 지역도 혁신적 약물에 대한 긴 승인 절차로 인해 발생하는 특허 보호 기간 손실을 보상하기 위해 유사한 제도를 구축했습니다.
2020년 1월 15일, 중국은 미국과 경제 무역 협정에 서명하여 특허 허가 또는 의약품 마케팅 승인 절차의 부당한 지연으로 인해 발생하는 손실을 보상하기 위해 중국의 특허법에 특허 기간 연장 제도를 추가하기로 합의했습니다. 2021년 6월, 개정 특허법이 정식으로 시행됨에 따라, 중국에서 특허기간 연장 제도가 본격적으로 시행되기 시작했습니다. 새로운 시행 규칙과 특허 심사 지침은 2024년 1월 20일에 시행되어 중국의 특허 기간 연장에 대한 시행 규칙을 자세히 설명하고 있습니다.
PTE 개요
- 개정된 특허법 제42조 제3항은 신약 출시 승인에 소요되는 시간을 보상하기 위해 중국 국가지식산권국(CNIPA)이 특허권자의 요청에 따라 중국에서 출시 승인을 받은 신약과 관련된 발명 특허의 기간을 연장할 수 있다고 규정하고 있습니다. 특허기간의 연장은 5년을 초과할 수 없으며, 연장 후의 총 유효 특허기간은 신약의 판매 승인일로부터 14년을 초과할 수 없습니다.
- 이 규정의 목적은 혁신적 약물 개발에 드는 높은 비용과 긴 주기를 균형 있게 조절하여 제약 회사가 특허 보호 기간 동안 R&D 투자를 합리적으로 회수할 수 있도록 보장하는 동시에, 더 많은 새로운 약물 혁신을 장려하고 회사의 R&D 열정을 높이는 것입니다.
특허기간 연장(PTE) 적용 약물
- 특허기간 연장은 '신약'에 함유된 활성 약제성분(API)과 관련된 제품특허, 제조공정특허, 의학적 사용특허에 적용됩니다. "신약"이란 국가약품감독관리총국(NMPA)의 약물 규제법 및 규정에서 정의한 혁신적 약물 및 일부 개량된 신약을 말합니다. 중국에서 특허 기간 연장을 위한 "신약"으로 인정받으려면 해당 약물이 전 세계적으로 신제품이어야 합니다. 즉, 다른 국가에서 마케팅 승인을 받기 전에 중국에서 신약 허가 신청(NDA)을 제출해야 합니다. 하지만 NDA는 다른 국가에서 승인을 받기 전에 반드시 중국에서 승인을 받아야 하는 것은 아닙니다.
PTE 조건을 충족하는 혁신적 약물:
- 현행 NMPA 의약품 분류 규정에 따르면 혁신 의약품은 1등급 의약품을 말하며, 세계적으로 새로운 의약품이어야 합니다. 적격한 혁신 약물에는 중국이나 해외에서 아직 승인되지 않은 다음 약물이 포함됩니다.
- 화학 약물;
- 예방 생물학적 제품 - 백신
- 치료용 생물학적 제품
- 전통 중의학.
PTE 조건을 충족하는 개량된 신약:
- 개량신약은 또한 세계적으로 새로운 것이어야 하며, NMPA의 약물 분류 규정에 따라 다음 약물로 제한됩니다.
- 2.1 화학 약물의 알려진 API의 에스테르 또는 염
- 2.4등급 화학의약품의 새로운 적응증이 있는 알려진 API
- 예방용 생물학적 제품의 2.2 범주에 속하는 변형된 박테리아 또는 바이러스 균주를 함유한 백신;
- 치료생물학적제품 2.2 카테고리의 새로운 적응증을 가진 치료생물학적제품
- 2.3등급에 속하는 한약재 중 기능이나 적응증이 강화된 것.
PTE에 적합하지 않은 약물:
- 위의 '신약' 정의에 따르면, 수입약품(즉, 중국에서 마케팅 승인을 신청할 때 해외에서 출시된 약물)은 PTE 조건을 충족하지 않습니다. 구체적으로는 5.1등급 화학의약품, 3.1등급 및 3.2등급 예방생물의약품, 3.1등급 및 3.2등급 치료생물의약품이 포함됩니다.
이러한 규정은 전 세계적으로 최초로 출시되거나 현저하게 개선된 약물만 특허 기간 연장의 대상이 되도록 보장하여 진정한 혁신과 고품질 개선을 장려합니다.
특허기간 연장(PTE)이 가능한 약물의 종류는 아래 표에 요약되어 있습니다.
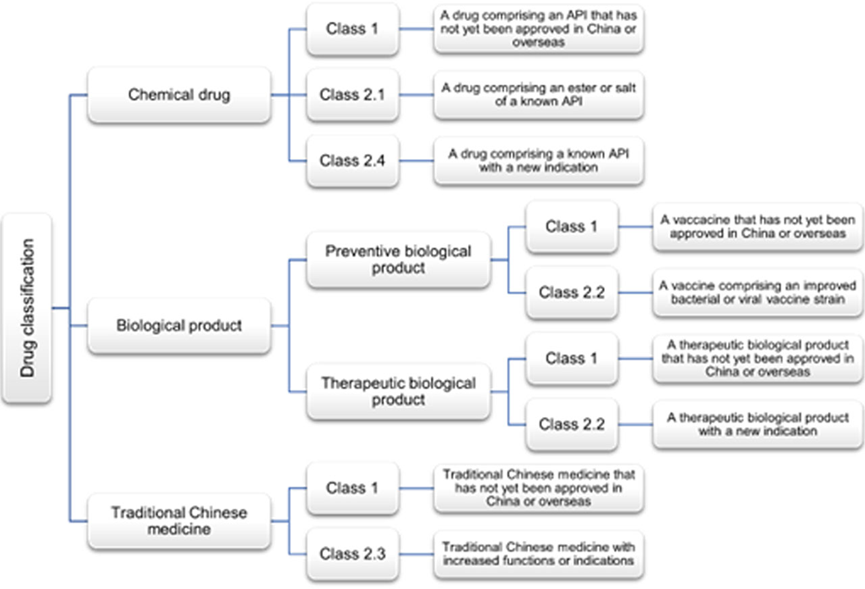
PTE 지원 기간 제한
- 특허 소유자 또는 그의 대리인은 약물에 대한 마케팅 승인을 받은 후 3개월 이내에 특허 기간 연장(PTE)을 요청하고 공식 수수료를 지불해야 합니다. 신청은 마케팅 승인 보유자의 승인 후에 이루어져야 합니다.
PTE 취득을 위한 요구사항
- 중국에서 PTE를 취득하려면 다음 요구 사항을 충족해야 합니다.
- 특허의 부여일은 약물의 승인일보다 빨라야 합니다.
- PTE 요청을 제출할 때, 특허는 유효한 상태여야 합니다.
- 해당 특허는 아직 PTE를 취득하지 못했습니다.
- 특허 청구항에는 약물과 관련된 기술적 솔루션이 포함되어야 합니다. 이러한 기술적 솔루션에는 승인된 신약의 구조, 구성 및 복용량은 물론 승인된 제조 공정 및 적응증이 포함됩니다.
- 해당 약물이 여러 개의 특허로 보호되는 경우, 하나의 특허의 기간만 연장될 수 있습니다.
- 특허가 여러 개의 약물을 포함하는 경우, PTE는 그 중 하나의 약물에만 신청될 수 있습니다.
PTE 시간 제한 계산
- PTE는 특허 기간 조정(PTA)에 더해 추가로 계산되는 사항이며, PTE 계산은 PTA 결정이 내려진 후에 수행되어야 합니다. 보상 사유가 다양하기 때문에 PTA와 PTE의 보상 기간이 누적될 수 있습니다.
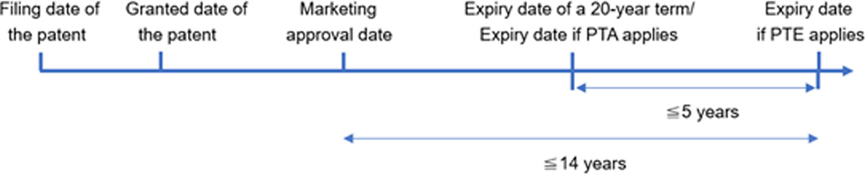
- PTE는 중국 특허 출원일과 중국 의약품 마케팅 승인일 사이의 일수에서 5년을 뺀 값으로 계산됩니다. 동시에 PTE는 다음 두 가지 요구 사항을 충족해야 합니다. 최대 PTE 기간은 5년이며, 약물이 마케팅 승인을 받은 후 총 유효 특허 기간은 14년을 초과할 수 없습니다.
PTE 요청 검토
- 심사관은 PTE 보상을 허가할지 여부를 결정하기 전에 특허 소유자에게 최소한 한 번의 의견 제시 또는 수정 기회를 제공합니다. PTE 요건이 충족되면 CNIPA는 PTE를 부여하고, 특허 기간이 연장되는 일수를 통지하고, 약물 이름, 승인된 적응증, 특허의 원래 만료일과 새로운 만료일과 같은 정보를 특허 공보에 게시합니다. CNIPA의 결정에 불만이 있을 경우, 특허권자나 이해관계가 있는 제3자는 행정 심사를 제기할 수 있습니다.
PTE 기간 동안의 보호 범위
- PTE의 목적은 신약의 마케팅 승인에 소요되는 시간을 보상하는 것이므로, 승인된 신약과 PTE가 신청된 약물 특허의 기술적 해결책을 직접적으로 연계시키는 것이 필요합니다. 신약과 관련된 기술적 솔루션은 출시된 신약과 PTE가 적용되는 약물 특허 사이의 다리 역할을 할 것입니다.
- PTE의 보호 범위는 특허 자체보다 좁으며, 승인된 적응증이 있는 신약에 한합니다. 즉, PTE의 보호 범위에는 다음이 포함됩니다.
- 승인된 적응증에 대한 제품 청구의 새로운 의약품
- 의료용으로 승인된 적응증이 있는 신약
- NMPA에 기록된 승인된 적응증에 대한 신약의 제조 공정입니다.
- 새로운 적응증은 새로운 PTE를 뒷받침할 수 있지만, 획득한 PTE의 범위는 PTE의 기반이 되는 새로운 적응증에만 적용되며, 이전이나 이후에 승인된 적응증에는 적용되지 않습니다.
- 따라서 특허권자는 PTE 신청서를 제출할 때 승인된 약물의 구성을 보여주는 자료, 승인된 약물의 적응증을 보여주는 자료, NMPA가 승인한 약물 제조 공정에 대한 자료 등 PTE의 보호 범위를 결정할 수 있는 자료를 제공해야 합니다.
결론적으로
혁신적인 제약 회사는 중국의 PTE 시스템을 적극적으로 활용하여 특허 기간 연장을 신청해야 합니다. 혁신적인 약물 회사는 PTE 요청을 제출할 때 청구 유형, 청구 범위, 특허의 안정성, 특허 집행, PTE 범위 및 "한 약물, 한 특허, 한 PTE" 규칙과 같은 모든 요소를 고려하여 하나 이상의 특허에 대한 특허 기간 연장을 극대화하고 합리화해야 합니다.
제네릭 의약품 회사의 경우, 혁신 의약품의 특허 기간을 연장하면 필연적으로 제네릭 의약품이 시장에 출시되는 시간이 지연될 것입니다. 이는 중국 내 많은 제네릭 의약품 회사에 상당한 영향을 미칠 것입니다. 제네릭 의약품 회사는 혁신적인 의약품 회사의 특허 만료일을 주의 깊게 살펴야 하며, NDA 절차를 간소화하기 위한 전략적 계획을 세워야 합니다. 필요하다면 제네릭 의약품 회사는 혁신적 의약품 회사의 특허에 대한 무효화 요청 제출을 고려할 수도 있습니다.
제네릭 의약품의 시장 출시가 늦어지면 약물 사용자 수수료가 인상될 것입니다. 특허 출원인은 혁신적인 제약 회사와 제네릭 제약 회사의 이익을 균형 있게 조정하고자 할 때 특히 중요합니다. 이러한 균형은 PTE에 관한 특허법과 시행 규정을 제정할 때 고려되었으며 PTE 취득을 위한 몇 가지 요건에 반영되었습니다. 예를 들어, 요구 사항에는 PTE를 취득하지 않은 특허만 PTE를 받을 수 있다는 것, 약물이 여러 특허로 보호되는 경우 특허를 하나만 연장할 수 있다는 것, 특허가 여러 약물을 포함하는 경우 특허는 그 중 하나의 약물에 대한 PTE만 신청할 수 있다는 것이 포함됩니다. 또한, 특허권의 최대 존속기간은 5년으로 규정하고 있으며, 의약품의 판매승인 이후 총 유효 특허기간은 14년을 초과할 수 없다고 규정하고 있습니다. 이러한 요구 사항은 혁신적인 제약 회사의 특허 기간에 대한 중복 보상을 효과적으로 피할 뿐만 아니라 특허 기간의 과도한 연장도 방지합니다.
联系咨询
 | Get exact prices For the country / regionE-mail: mail@yezhimaip.com |

