Le système de prolongation de la durée des brevets trouve son origine dans la loi américaine de 1984 sur la concurrence des prix des médicaments et la restauration de la durée des brevets (loi Hatch-Waxman). Par la suite, de nombreux pays ou régions comme le Japon, la Corée du Sud, l’Union européenne et le Canada ont également mis en place des systèmes similaires pour compenser la perte de période de protection des brevets causée par le long processus d’approbation des médicaments innovants.
Le 15 janvier 2020, la Chine a signé un accord économique et commercial avec les États-Unis, acceptant d'ajouter un système de prolongation de la durée des brevets à la loi chinoise sur les brevets pour compenser les pertes causées par des retards déraisonnables dans le processus d'autorisation de brevet ou d'approbation de la mise sur le marché de médicaments. En juin 2021, la loi révisée sur les brevets est officiellement entrée en vigueur et le système de prolongation de la durée des brevets a officiellement commencé à être mis en œuvre en Chine. Les nouvelles règles de mise en œuvre et les lignes directrices d'examen des brevets sont entrées en vigueur le 20 janvier 2024, détaillant les règles de mise en œuvre de la prolongation de la durée des brevets en Chine.
Présentation du PTE
- L'article 42, paragraphe 3, de la loi révisée sur les brevets prévoit que, afin de compenser le temps consacré à l'approbation de la commercialisation d'un nouveau médicament, l'Administration nationale chinoise de la propriété intellectuelle (CNIPA) peut, à la demande du titulaire du brevet, prolonger la durée des brevets d'invention liés à de nouveaux médicaments qui ont été approuvés pour la commercialisation en Chine. La prolongation de la durée du brevet ne doit pas dépasser cinq ans et la durée effective totale du brevet après prolongation ne doit pas dépasser 14 ans à compter de la date d'approbation du nouveau médicament pour la commercialisation.
- Ce règlement vise à équilibrer le coût élevé et le long cycle de développement de médicaments innovants, en garantissant que les sociétés pharmaceutiques puissent raisonnablement récupérer leurs investissements en R&D pendant la période de protection du brevet, tout en encourageant davantage d'innovations en matière de médicaments et en augmentant l'enthousiasme des entreprises en matière de R&D.
Médicaments concernés par la prolongation de la durée du brevet (PTE)
- La prolongation de la durée des brevets s’applique aux brevets de produits, aux brevets de procédés de préparation et aux brevets d’utilisation médicale liés aux principes pharmaceutiques actifs (API) contenus dans les « nouveaux médicaments ». Les « nouveaux médicaments » font référence aux médicaments innovants et à certains nouveaux médicaments améliorés tels que définis dans les lois et réglementations réglementaires sur les médicaments de la National Medical Products Administration (NMPA). Pour qu'un médicament soit qualifié de « nouveau médicament » et puisse bénéficier d'une prolongation de la durée du brevet en Chine, il doit être nouveau à l'échelle mondiale, ce qui signifie qu'une demande de nouveau médicament (NDA) doit être soumise en Chine avant d'obtenir l'approbation de mise sur le marché dans d'autres pays. Toutefois, il n’est pas nécessaire que la NDA soit approuvée en Chine avant de pouvoir être approuvée dans d’autres pays.
Médicaments innovants répondant aux conditions PTE :
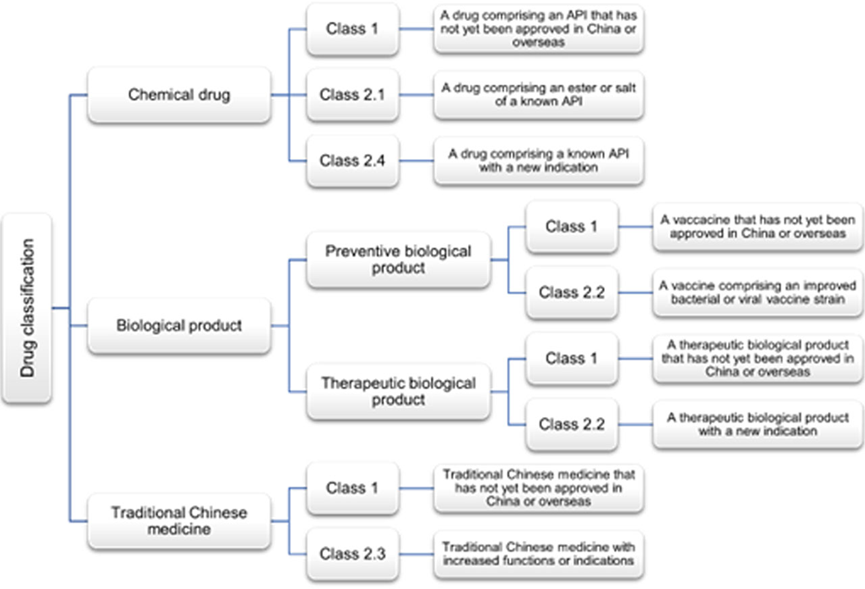
- Conformément à la réglementation actuelle de classification des médicaments de la NMPA, les médicaments innovants font référence aux médicaments de classe 1 et doivent être nouveaux à l'échelle mondiale. Les médicaments innovants éligibles comprennent les médicaments suivants qui n’ont pas encore été approuvés en Chine ou à l’étranger :
- Médicaments chimiques;
- produits biologiques préventifs – vaccins ;
- Produits biologiques thérapeutiques;
- médecine traditionnelle chinoise.
Nouveaux médicaments améliorés répondant aux conditions PTE :
- Les nouveaux médicaments améliorés doivent également être nouveaux à l’échelle mondiale et, conformément aux réglementations de classification des médicaments de la NMPA, se limitent aux médicaments suivants :
- Esters ou sels d’API connus de la classe 2.1 des médicaments chimiques ;
- API connues avec de nouvelles indications dans les médicaments chimiques de classe 2.4 ;
- Vaccins contenant des souches bactériennes ou virales modifiées de la catégorie 2.2 des produits biologiques préventifs ;
- Produits biologiques thérapeutiques avec de nouvelles indications dans la catégorie 2.2 des produits biologiques thérapeutiques ;
- Médicaments traditionnels chinois de la catégorie 2.3 qui ont des fonctions ou des indications accrues.
Médicaments qui ne sont pas éligibles à l’ETP :
- Selon la définition ci-dessus de « nouveau médicament », les médicaments importés (c’est-à-dire les médicaments qui ont été commercialisés à l’étranger lors de la demande d’autorisation de mise sur le marché en Chine) ne répondent pas aux conditions PTE. Il s’agit notamment des médicaments chimiques de classe 5.1, des produits biologiques préventifs de classe 3.1 et 3.2 et des produits biologiques thérapeutiques de classe 3.1 et 3.2.
Ces dispositions garantissent que seuls les médicaments qui sont les premiers du genre à l’échelle mondiale ou qui ont été considérablement améliorés sont éligibles à une prolongation de la durée de brevet, encourageant ainsi une véritable innovation et des améliorations de haute qualité.
Les catégories de médicaments éligibles à la prolongation de la durée du brevet (PTE) sont résumées dans le tableau ci-dessous :
Délai de candidature au PTE
- Le titulaire du brevet ou son mandataire doit déposer une demande de prolongation de la durée de validité du brevet (PTE) dans les trois mois suivant l'obtention de l'autorisation de mise sur le marché d'un médicament et payer la taxe officielle. La demande doit être déposée après l'autorisation du titulaire de l'autorisation de mise sur le marché.
Conditions requises pour l'obtention du PTE
- Pour obtenir un PTE en Chine, les exigences suivantes doivent être remplies :
- La date d’octroi du brevet doit être antérieure à la date d’approbation du médicament ;
- Lors de la soumission d’une demande de PTE, le brevet doit être en cours de validité ;
- Le brevet n'a pas encore obtenu de PTE ;
- Les revendications du brevet doivent inclure des solutions techniques liées au médicament ; ces solutions techniques comprennent la structure, la composition et le dosage du nouveau médicament approuvé, ainsi que le procédé de fabrication et les indications approuvés ;
- Si le médicament est protégé par plusieurs brevets, seule la durée d’un seul brevet peut être prolongée ;
- Si un brevet couvre plusieurs médicaments, un PTE ne peut être demandé que pour l’un d’entre eux.
Calcul du délai PTE
- Le PTE est un calcul supplémentaire en plus de tout ajustement de la durée du brevet (PTA) et le calcul du PTE doit être effectué après la prise de décision du PTA. En raison des différentes raisons d'indemnisation, les périodes d'indemnisation du PTA et du PTE peuvent être cumulées.
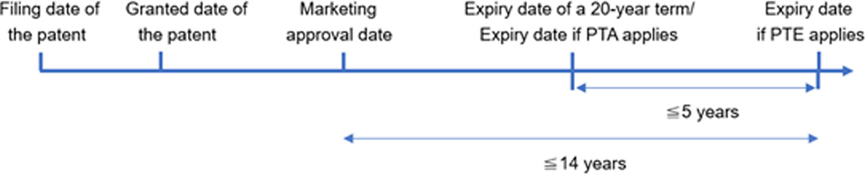
- Le PTE est calculé en soustrayant cinq ans du nombre de jours entre la date de dépôt du brevet chinois et la date d'approbation de la commercialisation du médicament chinois. Dans le même temps, le PTE doit répondre aux deux exigences suivantes : la durée maximale du PTE est de cinq ans et la durée totale effective du brevet après l'approbation de la commercialisation du médicament ne doit pas dépasser 14 ans.
Examen de la demande PTE
- Avant de décider d’accorder ou non une compensation PTE, l’examinateur donnera au titulaire du brevet au moins une occasion de faire des commentaires ou des modifications. Si les conditions requises pour le PTE sont remplies, le CNIPA accordera le PTE, notifiera le nombre de jours de prolongation de la durée du brevet et publiera des informations telles que le nom du médicament, les indications approuvées et les dates d'expiration originales et nouvelles du brevet dans la Gazette des brevets. Si le titulaire du brevet ou un tiers intéressé n'est pas satisfait de la décision du CNIPA, il peut déposer un recours administratif.
Étendue de la protection pendant la période PTE
- Étant donné que le but du PTE est de compenser le temps consacré à l’approbation de la mise sur le marché de nouveaux médicaments, il est nécessaire de lier directement le nouveau médicament approuvé à la solution technique du brevet de médicament pour lequel le PTE est demandé. Les solutions techniques liées aux nouveaux médicaments serviront de pont entre les nouveaux médicaments qui ont été lancés et les brevets de médicaments pour lesquels le PTE est appliqué.
- La portée de la protection d'un PTE est plus étroite que celle d'un brevet lui-même, limitée aux nouveaux médicaments ayant des indications approuvées, ce qui signifie que la portée de la protection d'un PTE comprend :
- Nouveaux produits pharmaceutiques dans les revendications de produits pour des indications approuvées ;
- Nouveaux médicaments avec des indications approuvées dans les revendications d’utilisation médicale ;
- Le processus de fabrication de nouveaux médicaments pour des indications approuvées enregistrées par la NMPA.
- Une nouvelle indication peut soutenir un nouveau PTE, mais la portée du PTE obtenu ne couvrira que la nouvelle indication sur laquelle le PTE est basé et non aucune indication approuvée antérieurement ou ultérieurement.
- Par conséquent, lors de la soumission d'une demande de PTE, le titulaire du brevet doit fournir des documents permettant de déterminer l'étendue de la protection du PTE, tels que des documents montrant la composition du médicament approuvé, des documents montrant les indications du médicament approuvé et des documents sur le processus de fabrication du médicament approuvé par la NMPA.
en conclusion
Les sociétés pharmaceutiques innovantes devraient utiliser activement le système PTE chinois pour demander une prolongation de la durée de leurs brevets. Lors du dépôt d'une demande de PTE, les sociétés pharmaceutiques innovantes doivent prendre en compte tous les facteurs, tels que le type de revendications, la portée des revendications, la stabilité du brevet, l'application du brevet, la portée du PTE et la règle « un médicament, un brevet, un PTE » pour maximiser et rationaliser la prolongation de la durée du brevet pour un ou plusieurs brevets.
Pour les sociétés de médicaments génériques, la prolongation de la durée de brevet des médicaments innovants retardera inévitablement le moment où les médicaments génériques entreront sur le marché, ce qui aura un impact significatif sur de nombreuses sociétés de médicaments génériques en Chine. Les sociétés de médicaments génériques doivent prêter une attention particulière aux dates d’expiration des brevets des sociétés pharmaceutiques innovantes et planifier stratégiquement la rationalisation de leurs calendriers de demande de nouveaux médicaments. Si nécessaire, les sociétés de médicaments génériques peuvent également envisager de déposer des demandes d'invalidation contre les brevets des sociétés de médicaments innovants.
L’entrée tardive des médicaments génériques sur le marché entraînera une augmentation des frais d’utilisation des médicaments. Les demandeurs de brevets sont particulièrement importants lorsqu’ils cherchent à équilibrer les bénéfices des sociétés pharmaceutiques innovantes et des sociétés de médicaments génériques. Cet équilibre a été pris en compte lors de la formulation de la loi sur les brevets et de son règlement d’application concernant le PTE et se reflète dans plusieurs exigences pour l’obtention d’un PTE. Par exemple, les exigences incluent que seuls les brevets qui n’ont pas obtenu de PTE sont éligibles à un PTE ; si un médicament est protégé par plusieurs brevets, un seul brevet peut être prolongé ; et si un brevet couvre plusieurs médicaments, le brevet ne peut demander un PTE que pour l’un des médicaments. En outre, il est également stipulé que la durée maximale du PTE est de cinq ans et que la durée totale effective du brevet après l'approbation du médicament pour la commercialisation ne doit pas dépasser 14 ans. Ces exigences permettent non seulement d’éviter efficacement la double rémunération des durées de brevets versées aux sociétés pharmaceutiques innovantes, mais également d’empêcher une prolongation excessive de la durée des brevets.
 | Get exact prices For the country / regionE-mail: mail@yezhimaip.com |

